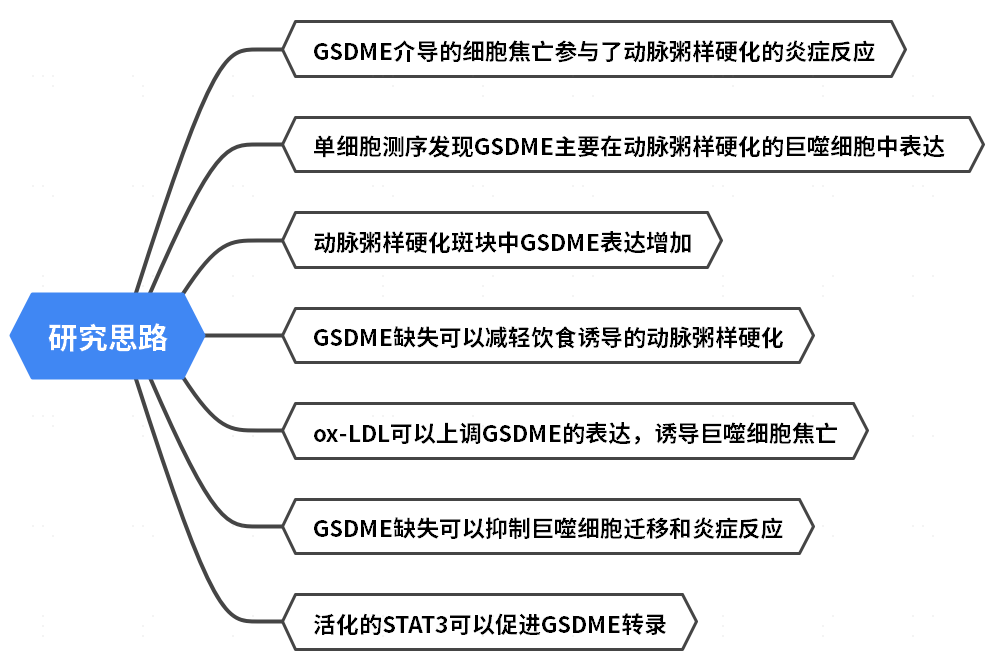
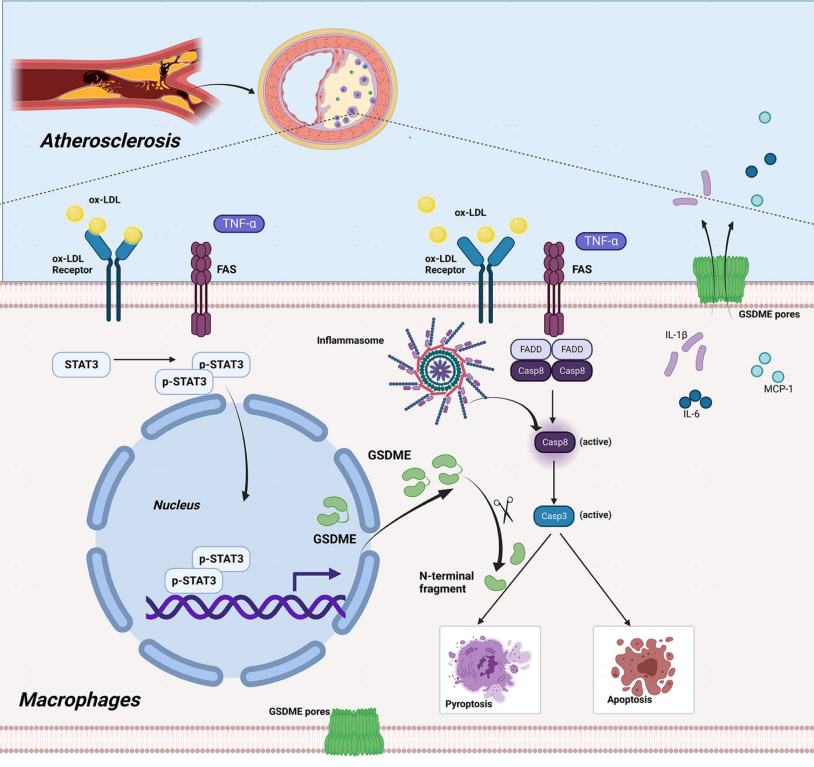
1.细胞焦亡参与人和小鼠的动脉粥样硬化进程
为了探索动脉粥样硬化的超微结构,作者从接受颈动脉内膜切除术的患者中获得了动脉粥样硬化斑块组织,通过透射电镜观察发现大量巨噬细胞死于细胞焦亡而非凋亡过程。免疫组化结果显示,与对照血管相比,动脉粥样硬化组中IL-1β、caspase 3和GSDME表达水平升高。使用邻近连接技术检测GSDME和caspase 3在动脉粥样硬化斑块中的相互作用并评估GSDME激活和caspase 3介导的细胞焦亡,发现整体蛋白的相互作用与IL-1β免疫组化的信号分布模式相似,表明由GSDME介导的细胞焦亡参与了动脉粥样硬化的炎症反应。

图1 人和小鼠动脉粥样硬化斑块中的细胞焦亡
2.GSDME主要在动脉粥样硬化组织中的巨噬细胞表达
为了研究人类动脉粥样硬化斑块的转录组特征以及GSDME在动脉粥样硬化中的表达情况,作者对接受颈动脉内膜切除术患者的颈动脉晚期粥样硬化病变组织进行了单细胞转录组测序。结果表明GSDME主要在M1巨噬细胞中表达,并进一步通过GSDME和巨噬细胞标记物CD68的共染证实GSDME定位于CD68标记的巨噬细胞中。GSEA分析发现M1巨噬细胞上调白细胞迁移相关基因,而M2巨噬细胞下调了免疫应答相关基因。这些发现揭示了细胞可塑性以及巨噬细胞GSDME的表达在人类晚期动脉粥样硬化进展中的突出作用。
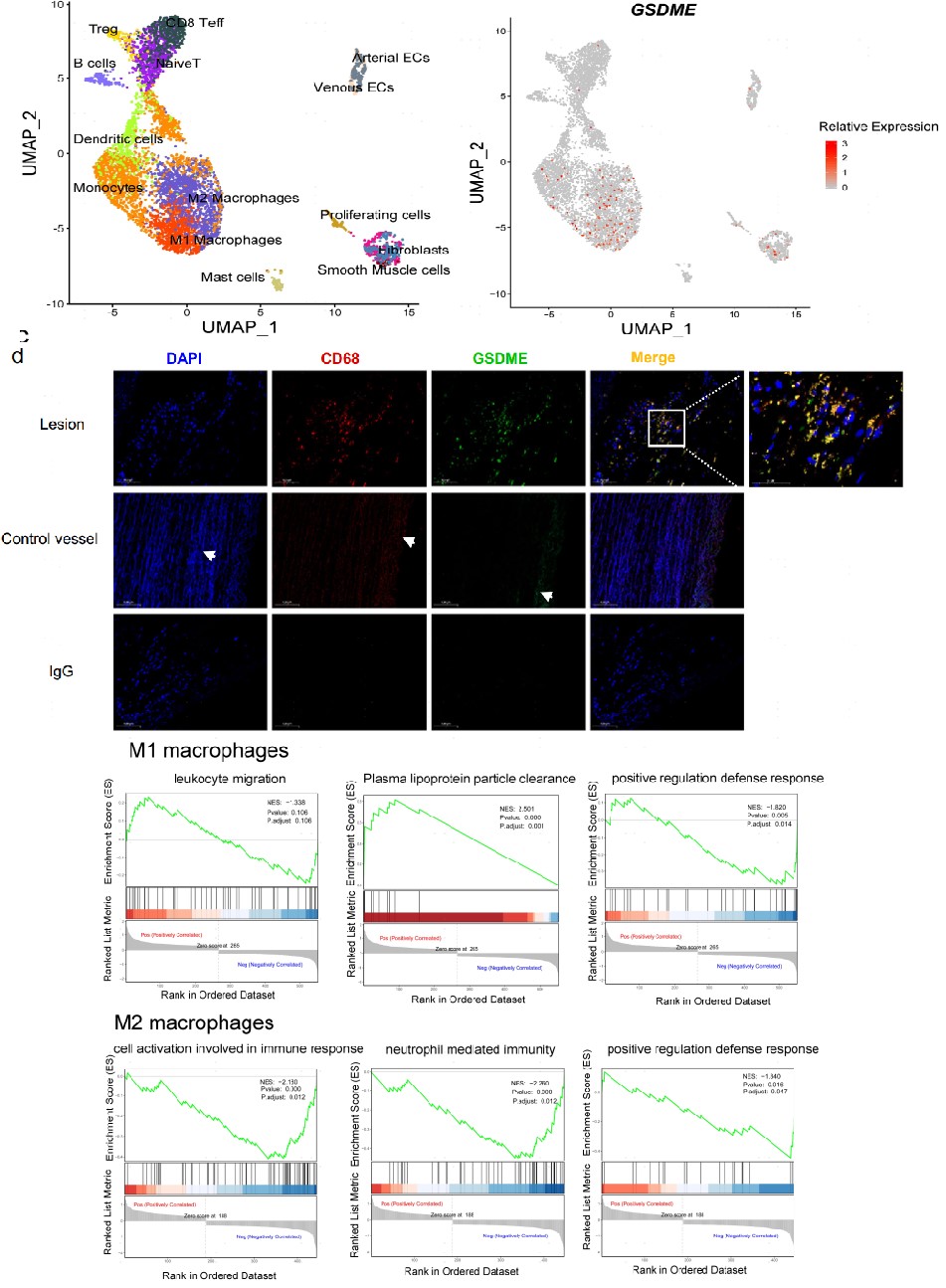
图2 GSDME主要表达在动脉粥样硬化组织的巨噬细胞中
3.在人和小鼠动脉粥样硬化斑块中GSDME表达增加
作者对GSE43292数据集中的32个人动脉粥样硬化斑块和邻近完整组织的基因表达数据进行分析发现GSDME在人动脉粥样硬化斑块中的表达显著增加,并通过Western blotting证实完整的GSDME和激活的GSDME(N-GSDME)蛋白水平在人晚期动脉粥样硬化病变中显著升高。在动脉粥样硬化易感的ApoE−/−小鼠中,经过12周的高脂饮食喂养后,GSDME的蛋白和mRNA水平均显著升高。与GSDME表达一致,在ApoE−/−小鼠的主动脉中促炎基因如:IL-1β、肿瘤坏死因子α、MCP-1和IL-6的mRNA水平也明显升高,表明GSDME在调节动脉粥样硬化斑块形成中起着关键作用。
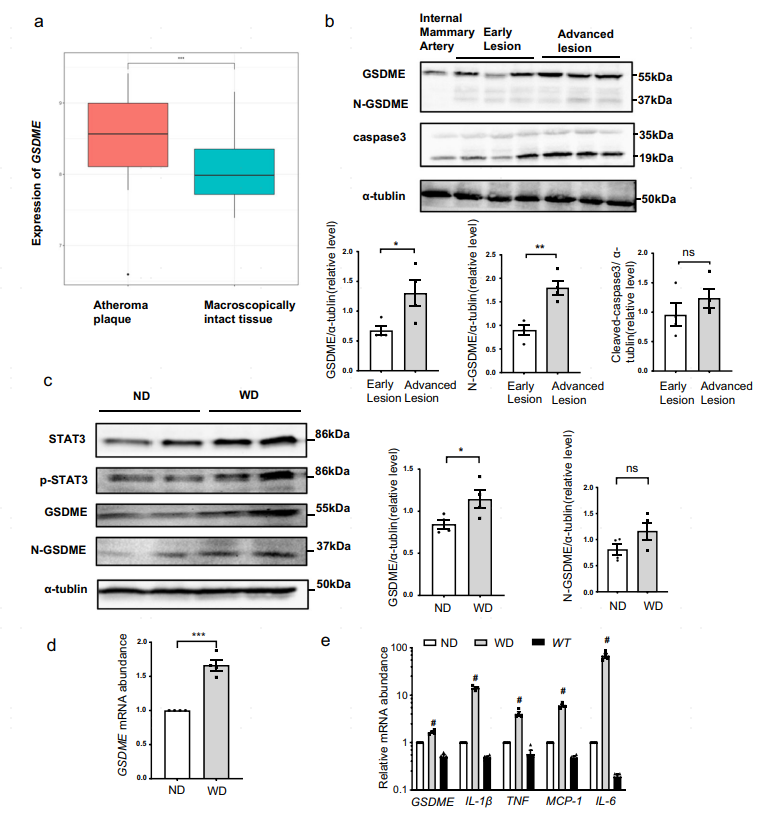
图3 GSDME在动脉粥样硬化组织中表达增加
4.ApoE−/−小鼠中GSDME缺失可以减轻饮食诱导的动脉粥样硬化
基于前述发现的GSDME在动脉粥样硬化中表达增加,作者想进一步探究GSDME缺失是否可以抑制动脉粥样硬化的进展。采用8周龄的GSDME−/−/ApoE−/−小鼠和对照组ApoE−/−小鼠,进行高脂饮食喂养12周后,两组小鼠血清HDL、LDL和胆固醇水平无显著差异,但GSDME−/−/ApoE−/−小鼠动脉粥样硬化病变面积较ApoE−/−小鼠减少28%。同时,与ApoE−/−小鼠相比,GSDME−/−/ApoE−/−小鼠的主动脉窦和头臂动脉病变大小、头臂动脉坏死病变面积均显著减小。此外,GSDME−/−/ApoE−/−小鼠主动脉中促炎基因如TNF、IL-1β、IL-6和MCP-1的mRNA水平显著降低。总的来说,这些结果表明GSDME缺失可以减轻ApoE−/−小鼠饮食诱导的动脉粥样硬化和炎症反应。
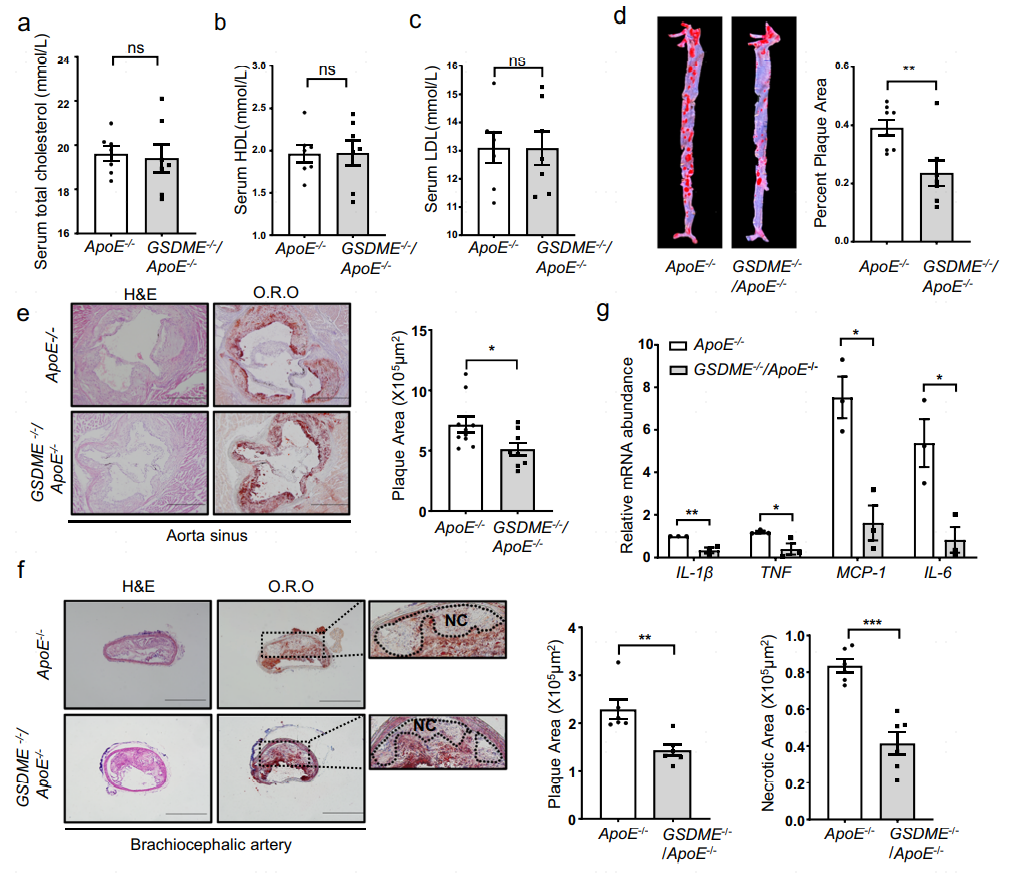
图4 GSDME缺失可以减小动脉粥样硬化病变的面积
5.Ox-LDL诱导巨噬细胞GSDME表达和细胞焦亡
将原代腹腔巨噬细胞(PMs)和骨髓来源的巨噬细胞(BMDMs)与ox-LDL孵育24小时后,PMs和BMDMs中均出现GSDME表达水平增加。为了评估ox-LDL诱导巨噬细胞焦亡的程度,作者检测了释放到培养基中的乳酸脱氢酶(LDH)活性,结果表明ox-LDL以剂量依赖的方式促进细胞死亡,同时GSDME缺失降低了LDH的释放。这些结果表明ox-LDL可以上调GSDME的表达,诱导巨噬细胞焦亡,进而促进动脉粥样硬化的进展。
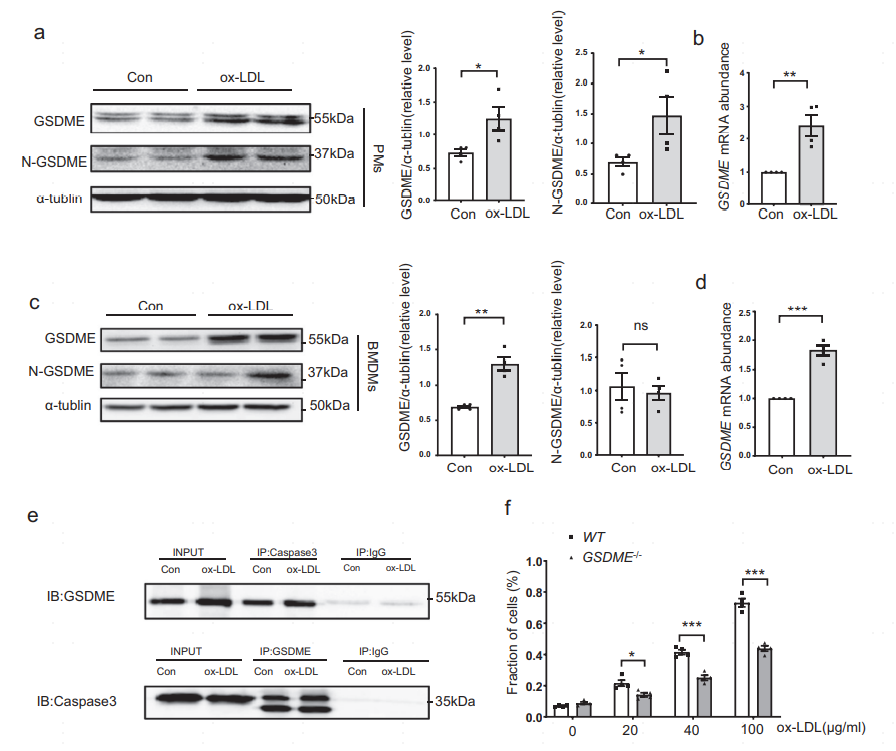
图5 ox-LDL诱导巨噬细胞中GSDME的表达
6.GSDME缺失可以抑制巨噬细胞迁移和炎症
作者使用ox-LDL处理WT或GSDME−/−小鼠的腹腔巨噬细胞来探究GSDME缺失是否可以减弱巨噬细胞的炎性行为。与对照组相比,GSDME−/−小鼠的细胞粘附相关基因:Lama2、Pcdhb和Itga7显著下调。细胞通过特定的粘附点粘附到基质是细胞迁移的关键,因此进一步通过Transwell和划痕实验发现GSDME缺失显著减少了巨噬细胞的迁移。鉴于动脉粥样硬化相关炎症反应是由促炎细胞因子、炎症信号通路和粘附分子介导的,作者探究了来自GSDME−/−和野生型小鼠的PMs经ox-LDL处理后的炎症反应。与预期一致,ox-LDL处理后的GSDME−/−组PMs中TNF、IL-1β、MCP-1等炎性基因表达出现显著下降,表明GSDME缺失可以抑制巨噬细胞的炎症反应和细胞焦亡。

图6 巨噬细胞GSDME缺失可以抑制其炎症反应和细胞焦亡
7.STAT3上调GSDME表达
STAT3激活可以参与动脉粥样硬化的炎症反应,因此靶向抑制STAT3可能是一种潜在的动脉粥样硬化治疗策略。与正常饮食组相比,高脂饮食组ApoE−/−小鼠主动脉中pSTAT3(磷酸化STAT3)水平显著升高。与GSDME相同,STAT3在人动脉粥样硬化巨噬细胞中也有一定程度的表达。在ox-LDL或caspase 3激活剂TNF处理的腹腔巨噬细胞中,GSDME和pSTAT3蛋白水平同时升高。通过过表达或敲降实验,作者发现STAT3与GSDME的表达直接相关,还进一步预测了GSDME基因启动子区域存在的4个STAT3结合位点。染色质免疫共沉淀实验证实了STAT3与包含一致序列TTCTGAGAAG的4个结合位点的结合增加,表明了STAT3在GSDME转录调节中的重要作用。
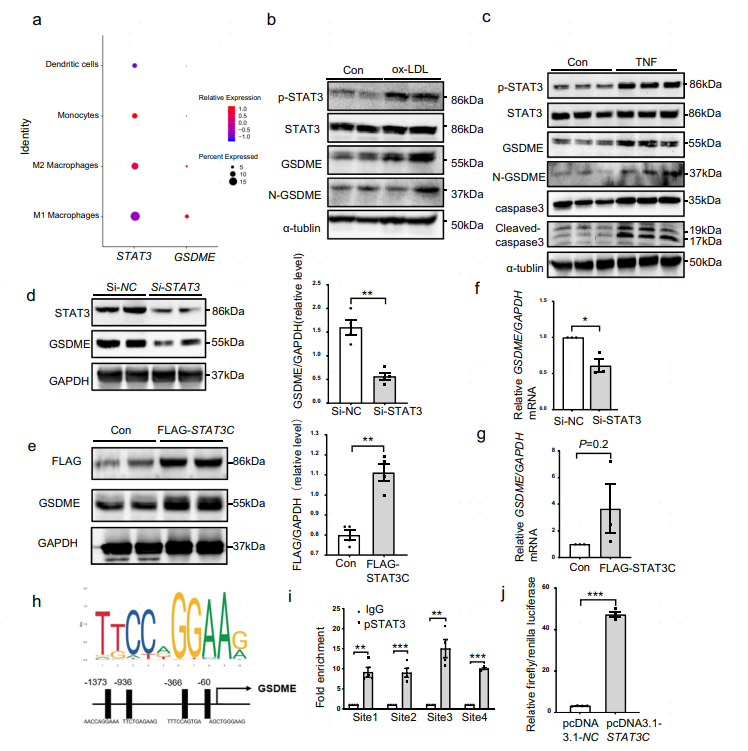
图7 STAT3靶向GSDME启动子并激活GSDME转录