新格元在该研究中提供了GEXSCOPE大孔芯片单细胞转录组测序试剂盒。
项目文章 | 新格元单细胞大孔芯片解密霍奇金淋巴瘤新靶点
发布时间:2024-10-10 10:18:05
知识卡片
新格元大孔芯片转录组试剂盒专为“大细胞”科研探索而生,包含大孔径微孔芯片,可高效捕获较大直径细胞类型,无需提核,即可全面获得细胞内转录组信息。
思维导图
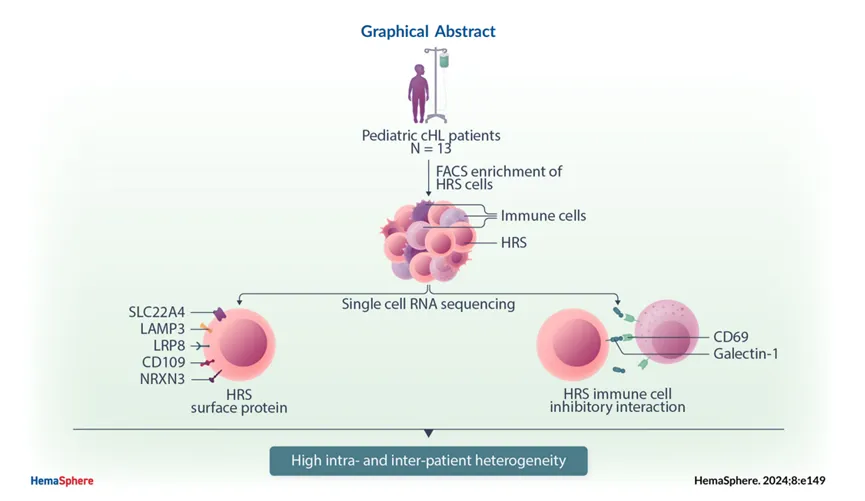
主要研究结果
1.scRNA-seq捕获HRS细胞
本研究分选13个儿童cHL淋巴结的HRS细胞,将3个非恶性反应性淋巴结(RLNs)作为对照,通过单细胞转录组测序和细胞注释,B和T淋巴细胞以及髓系细胞被鉴定出来(图1a)。根据典型亚型标记识别亚型,鉴定了疲惫和幼稚的CD8 T细胞,以及疲惫、循环和幼稚的CD4 T细胞和TFH细胞。检测NAIVE、PLAA和GC B细胞,以及单核细胞和巨噬细胞。不同的DCs亚群也被识别,包括成熟的、半透明的、CLEC9A+、CD1C+和CCR6+DCs(图1a)。
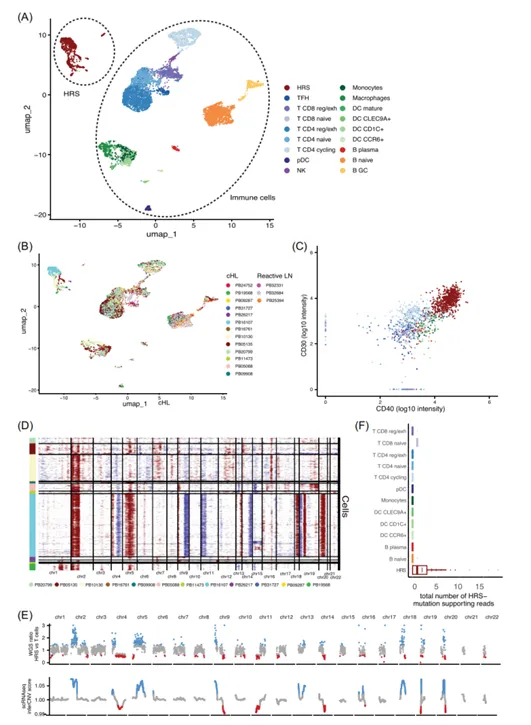
图1 通过单细胞测序捕获的HRS细胞
2.HRS细胞表面标志物的发现
作者在scRNA‐seq和两个微阵列数据集中对HRS细胞和健康B细胞进行了差异表达分析(DEA)。在三个数据集中965个基因在HRS细胞中一致过表达,并被称为“HRS核心”集(图2A,B)。为了确定潜在的治疗靶点,HRS核心基因被选择为高预测可能性存在于质膜上,仅在少数健康组织中表达,并且存在于至少≥80%cHL患者的HRS细胞上。除了已知的TNFRSF8(CD30)外,还发现了其他在HRS细胞中持续过表达的细胞表面蛋白基因,如NRXN3和LRP8,这些可能作为抗体-药物偶联物或CAR T细胞的替代靶点。
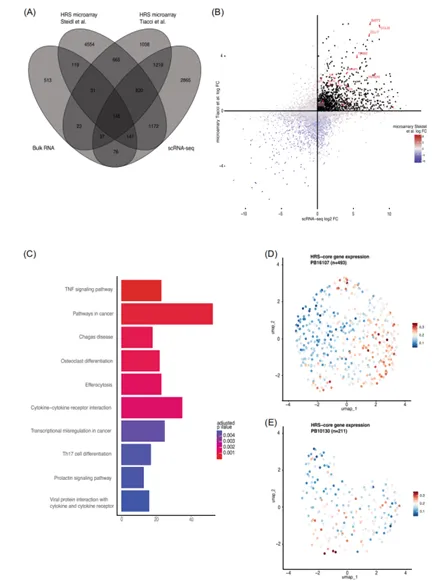
图2 HRS细胞核心基因
3.HRS与免疫细胞相互作用的识别
为了研究cHL中的细胞-细胞相互作用,使用scRNA-seq数据作为参考,对从诊断部门获得的59个cHL和14个RLN样本的bulk RNA-seq进行分析,发现耗尽的CD8+T细胞占大多数细胞。HRS细胞与T细胞之间的潜在抑制性相互作用,特别是通过galectin-1/CD69和HLA-II/LAG3相互作用。这些发现有助于理解HRS细胞如何在肿瘤微环境中抑制T细胞的活性。
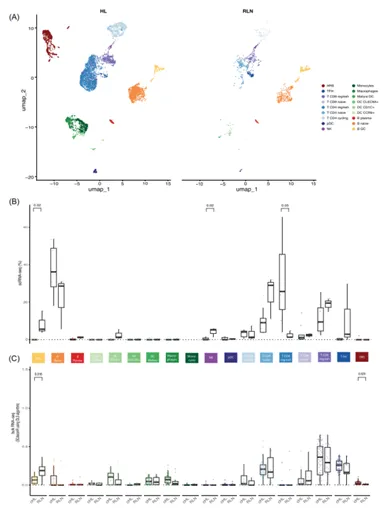
图3 cHL微环境的免疫细胞组成与反应性淋巴结的比较
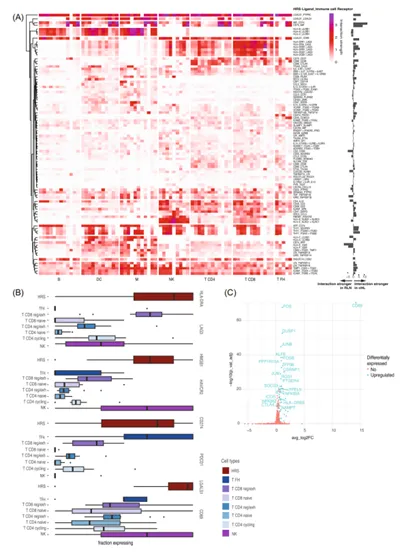
图4 HRS细胞与肿瘤微环境细胞之间的潜在相互作用
结论
与传统化疗相比,针对肿瘤的更有针对性的治疗方法的发展,因此对健康组织的毒性更小,可以改善儿科cHL幸存者的生活质量。本研究采用scRNA-seq技术,对分离的HRS细胞和免疫细胞进行测序。通过对TNFRSF8(CD30)的研究,作者发现了在HRS细胞中一致过表达的细胞表面蛋白的其他基因,如NRXN3和LRP8,它们可能被用作抗体-药物偶联物或CAR-T细胞的替代靶标。最后,作者确定了HRS细胞抑制T细胞的潜在相互作用,其中包括凝集素-1/CD69和HLA-II/LAG3相互作用。使用RNAscope验证了CD69和LAG3在HRS细胞附近的T细胞上的表达富集,并表明患者之间和肿瘤组织区域之间与相应配体的相互作用强度存在很大差异。
参考文献
de Kanter JK, Steemers AS, Montiel Gonzalez D, et al. Single‐cell RNA sequencing of pediatric Hodgkin lymphoma to study the inhibition of T cell subtypes. HemaSphere. 2024;8:e149. doi:10.1002/hem3.149








