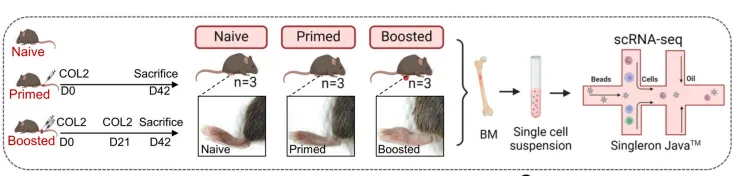
1.特定的中性粒细胞群的ROS代谢过程在实验性关节炎的发展中至关重要
BM是造血的主要部位,负责产生包括中性粒细胞在内的所有类型的血细胞,对于了解中性粒细胞在RA中的发育和功能至关重要。为了表征免疫启动和关节炎发病期间的中性粒细胞,对初始、免疫启动(第0天)和免疫增强(第21天重复COL2免疫)即关节炎发病期间的骨髓细胞进行了scRNA-seq分析。总共分析了72388个细胞,根据典型标志物的表达确定了10个不同的簇,包括B cells, plasma cells, HSCs, ProEryth,erythroblasts, GMP, neutrophils, basophils, T cells, MPs(图1A,B)。其中,中性粒细胞的比例在初始组和启动组之间差异显著(图1C,D)。然而,没有观察到幼稚组和增强组之间的显著差异,可能是因为增强小鼠的中性粒细胞更有效地募集到炎症部位,这表明中性粒细胞从BM迁移到组织而不通过血管室(图1C,D)。随后,用抗Ly6G抗体耗尽DBA1/J小鼠的中性粒细胞,随后用COL2免疫它们,发现只有中性粒细胞耗尽的小鼠发展为轻度关节炎,这表明中性粒细胞可以防止小鼠在CIA早期发展为关节炎(图1E,F)。为了剖析中性粒细胞的异质性,进一步研究了中性粒细胞相关人群(MPs和中性粒细胞)。无监督聚类将分化中性粒细胞和成熟中性粒细胞分成5个簇(G0-4)(图1G)。同样,初始、增强和原始小鼠的中性粒细胞数量从高到低排列(图1G)。单细胞轨迹分析显示中性粒细胞成熟和分化的时间过程高度一致,显示了中性粒细胞从GO到G4的发育轨迹(图S1D)。此外,观察到初始小鼠中向G4群体分化的细胞数量显著增加(图S1E)。在DEGs的GO分析中,细胞周期相关基因在中性粒细胞成熟的早期阶段(GO,G1和G2)高表达,氧化还原相关基因在噬菌体晚期(G3和G4)上调(图S1F-G)。G4细胞的GO富集分析显示,它们与ROS代谢过程的反应和炎症反应的调节密切相关(图1H)。在G4细胞中,NADPH类酶、ROS生成、趋化性、中性粒细胞激活和成熟评分在关节炎早期阶段显著上调(图S1H)。还发现G4亚群高表达Ncf1,Ncf1是NOX2复合体的重要亚基,负责诱导ROS,进一步支持中性粒细胞ROS的产生主要是由吞噬NADPH氧化酶在关节炎前期介导的(图1I-J)。
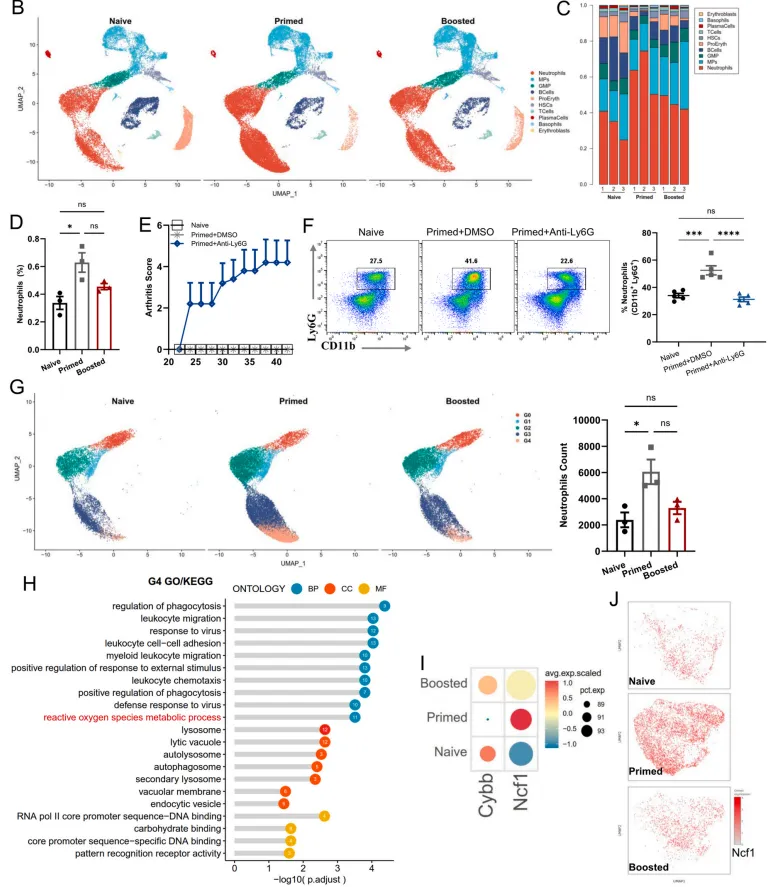
图1. 单细胞测序分析关节炎中BM中性粒细胞
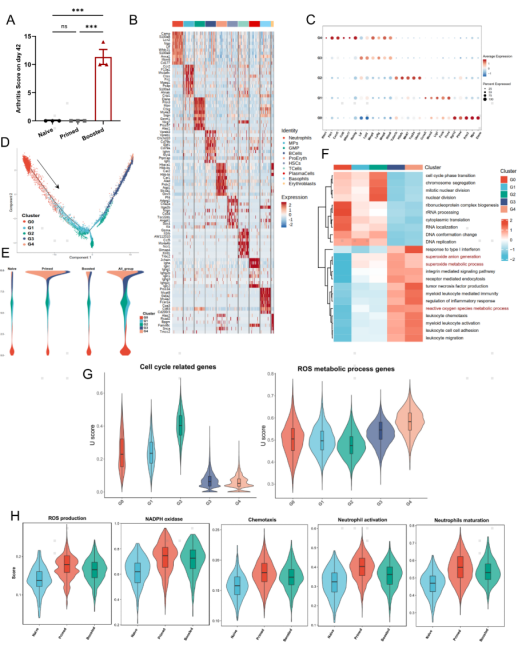
图S1. 关节炎中BM中性粒细胞亚群的特征
2.ROS在实验性关节炎的发展中显示出双重作用
在免疫启动过程中,ROS的丢失导致关节炎的发展,关节中中性粒细胞数量增加。相反,在关节炎发病期间,ROS的缺失通过减少中性粒细胞数量来缓解关节炎症状,提示ROS双向调节关节炎(图2)。
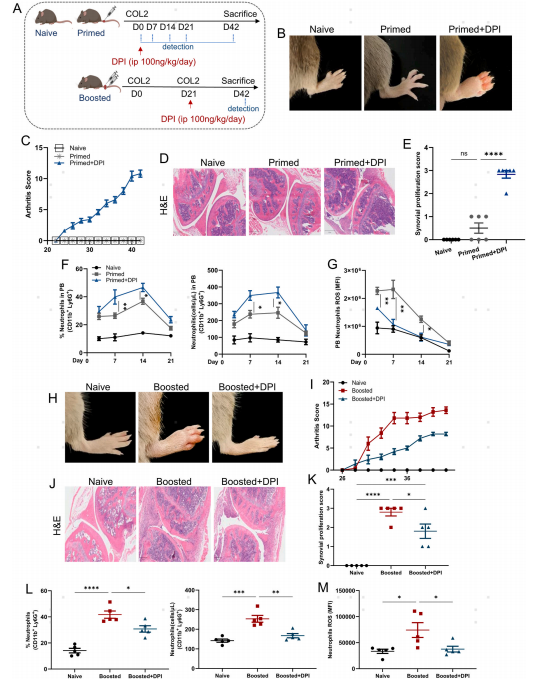
图2. ROS在关节炎的早期保护和晚期发病中起双向作用
3.实验性关节炎早期中性粒细胞ROS缺乏会加重关节炎症
抑制NOX2来源的ROS后,初始小鼠对关节炎的易感性更高,表明中性粒细胞来源的ROS是一个重要的调节因子。实验性关节炎早期阶段的ROS缺乏促进中性粒细胞表现出促炎特性,从而促进关节炎的发展(图3)。
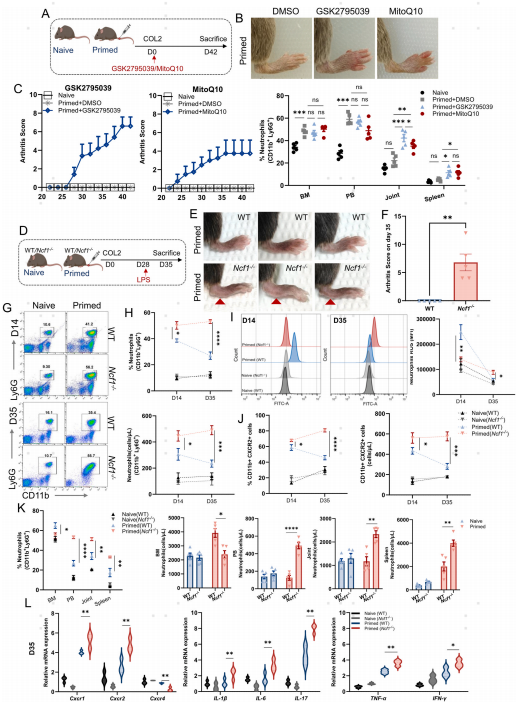
图3. ROS缺乏通过在早期募集中性粒细胞引发关节炎
4.ROS缺乏会影响中性粒细胞的功能
ROS缺乏的中性粒细胞通过减少氧化呼吸爆发、钙通量和形态不扩张来自我维持。这种ROS水平的改变导致中性粒细胞功能的改变,主要表现为迁移、跨血管内皮能力和炎症免疫反应的增加,以及吞噬和粘附的减少,以便快速迁移到炎症部位以发挥其作用(图4)。
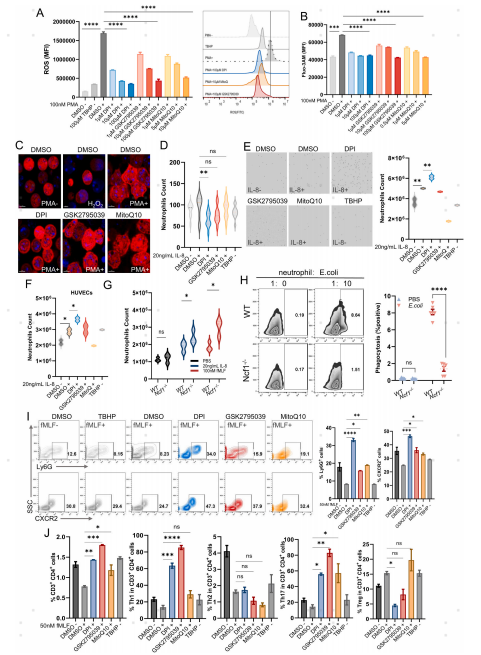
图4. 缺乏ROS时中性粒细胞功能和炎症表型的改变
5.ROS缺乏的中性粒细胞表现出更强的炎症代谢
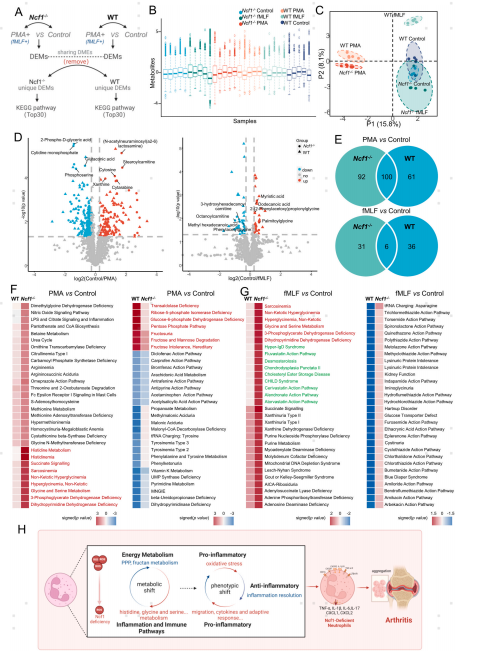
图5. ROS缺陷中性粒细胞的炎症代谢重编程