新品上市 | 新格元单细胞胞内菌检测技术重磅发布
发布时间:2024-12-27 11:22:01
单细胞测序2009年问世以来,一路生花:2013年被Nature Methods评为年度技术、2018年被Science评为年度突破技术,2019年再次被Nature Methods评选为年度技术。单细胞测序的强大生命力还体现在与其他组学结合研究基因表达与表型异质性之间的联系,例如与基因组结合,衍生出单细胞ATAC技术;与蛋白组结合,延伸出CITE-seq技术。
跨物种同时检测的技术是否可以实现呢?比如微生物组与单细胞测序的整合,细菌与宿主的互作,它的研究是否会是下一个“弄潮儿”?
细菌是一种肉眼虽看不见,但实实在在存在的微小生物,其与个体发育、免疫、神经、代谢稳态等方面息息相关。近年来,不断有文献报道结直肠癌、乳腺癌等在内的多种实体瘤内存在细菌,影响肿瘤的发生发展并可能导致患者耐药。2020年《Science》报道了乳腺癌、肺癌、卵巢癌、胰腺癌、黑色素瘤、骨癌、脑瘤7种癌症类型1526个肿瘤及邻近正常组织的肿瘤微生物组,发现每种肿瘤都有不同的菌群组成,同时瘤内细菌具有代谢活性,大部分位于细胞内,在癌细胞和免疫细胞中都存在[1]。2022年西湖大学蔡尚教授团队发现乳腺癌组织中存在多种独特的“胞内菌”,并证明胞内菌可以促进肿瘤细胞的转移,拥有胞内菌的肿瘤细胞具有更强的远端转移的能力[2]。2024年香港中文大学于君教授团队发现口腔微生物群成员厌氧消化链球菌除了加剧结直肠癌的发展,还能通过增强髓源性抑制细胞的活性,削弱抗PD1疗法对小鼠结直肠癌的疗效[3]。这些研究只是冰山一角,细菌与宿主之间是一场没有硝烟的战争,了解细菌对宿主细胞的影响是打赢这一场战争关键的一步。
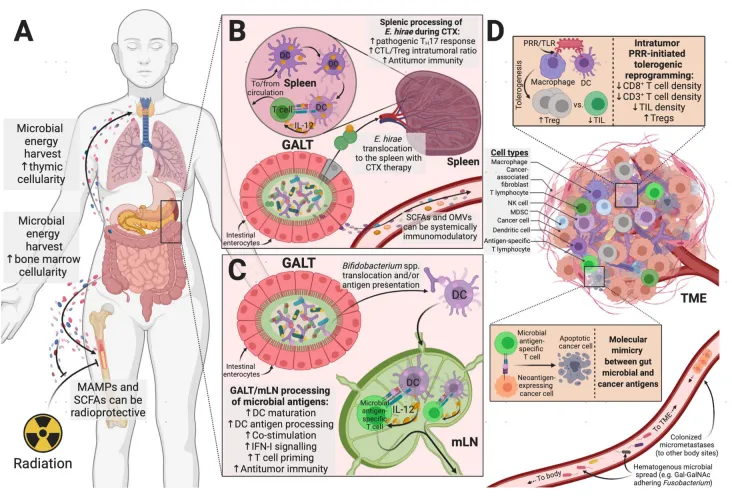
Sepich-Poore GD, et al. Science. 2021
微生物调节宿主代谢和免疫,最终影响肿瘤
标准的单细胞测序通过poly(dT)捕获mRNA的polyA尾,得到转录组数据,揭示细胞的异质性。而细菌mRNA往往缺少polyA尾,导致在标准单细胞测序中只能得到有限的细菌数据。新格元FocuSCOPE®靶向系列产品,可以对突变基因、融合基因、病毒与宿主RNA等研究热点区域进行特异性捕获。了解微生物和肿瘤之间的复杂关系可以为潜在和现有的癌症治疗方案提供有价值的见解,鉴于此,新格元推出FocuSCOPE®单细胞胞内菌检测技术服务,这一技术有望在刻画组织单细胞图谱和微生物菌群的同时,帮助研究者探索基于微生物干预的联合治疗策略,提高临床治疗效果。
FocuSCOPE®单细胞胞内菌检测技术,基于新格元的单细胞微流控系统分离细胞,对单细胞探针进行改良,在单细胞核酸捕获的寡核苷酸序列上加入靶向细菌16S目标位点的特异性探针,以同时捕获单个细胞的mRNA分子和胞内细菌信息,显著提高测序文库产物得率及同等测序深度下细菌的检出率FocuSCOPE®单细胞胞内菌检测技术,提供一站式服务,可快速完成从组织样本运输、解离制备单细胞悬液、单细胞分离、mRNA以及细菌16S转录本的定向捕获和NGS测序文库构建整体流程。
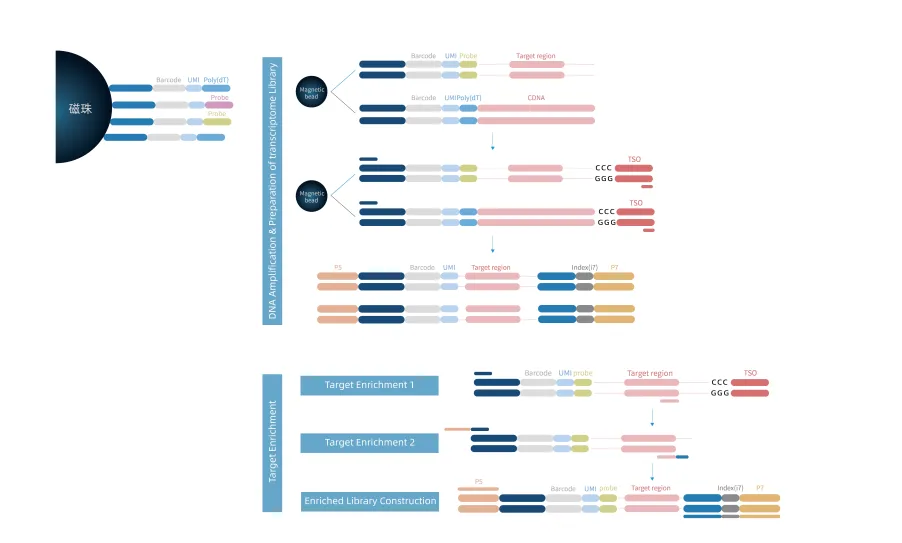
探针设计
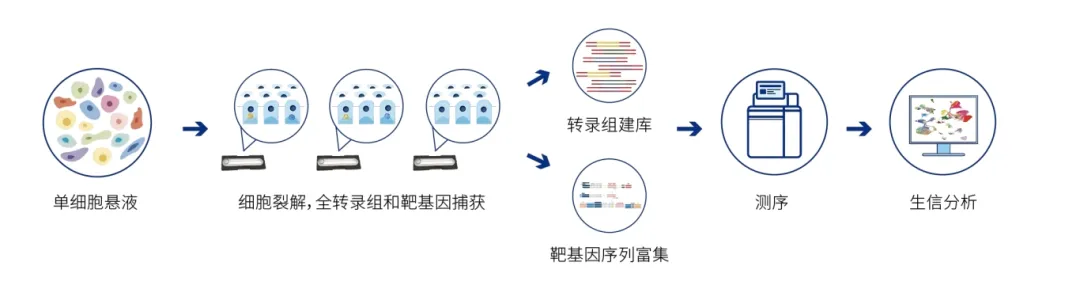
一站式FocuSCOPE®单细胞胞内菌检测方案
揭示存在于样本中的细菌种类,以及在细胞类型中的分布情况。
探究细菌--宿主细胞如何相互吸引、相互作用,甚至可能相互依赖的。
追踪在微环境中“作案”的细菌,揭露它们对宿主细胞的影响。
通过了解细菌如何促进肿瘤生长,从而发现新的治疗靶点,开发出更有效的抗癌策略。
了解细菌在肿瘤/疾病演变过程中的角色和影响。
了解细菌如何影响免疫细胞,从而改变肿瘤的命运。
[1]Neiman, D. et al. The human tumor microbiome is composed of tumor type-specific intracelular bacteria. Science. 2020 May 29;368(6494):973-980.
[2]Fu A, et al. Tumor-resident intracellular microbiota promotes metastatic colonization in breast cancer. Cell. 2022 Apr 14;185(8):1356-1372.e26.
[3]Liu Y, et al. Peptostreptococcus anaerobius mediates anti-PD1 therapy resistance and exacerbates colorectal cancer via myeloid-derived suppressor cells in mice. Nat Microbiol. 2024 Jun;9(6):1467-1482.
[4]Sepich-Poore GD, et al. The microbiome and human cancer. Science. 2021 Mar 26;371(6536):eabc4552. doi: 10.1126/science.abc4552. Erratum in: Science. 2024 Sep 27;385(6716):eadt2260.








